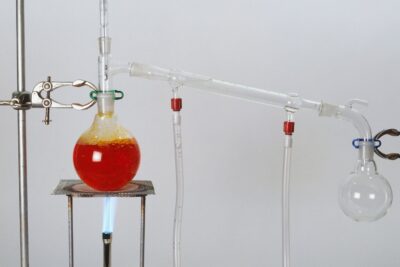
La sosa cáustica es uno de los nombres comunes para el hidróxido de sodio (NaOH), que también se conoce como lejía. Su nombre común deriva de su identidad química como hidrato de sodio y porque es cáustico o corrosivo. En forma pura, la sosa cáustica es un sólido blanco ceroso. Absorbe fácilmente el agua y forma soluciones acuosas. La sosa cáustica o el hidróxido de sodio disponibles en el mercado suelen ser hidróxido de sodio monohidratado, NaOH * H2O.
Conclusiones Clave: Soda Cáustica
- La sosa cáustica es uno de los nombres comunes para el hidróxido de sodio (NaOH).
- También se conoce como lejía, aunque la lejía puede referirse a hidróxido de potasio o hidróxido de sodio.
- La soda cáustica pura se vende para hacer velas o jabón.
- La sosa cáustica impura se encuentra en el limpiador de desagües.
- Debido a que la lejía se usa para fabricar drogas ilegales, es más difícil comprar grandes cantidades que en el pasado. Sin embargo, los recipientes pequeños están disponibles en tiendas y en línea.
Usos de Sosa Cáustica o Lejía
La lejía se usa para hacer jabón, hacer velas, biodiesel casero, glasear vidrio, hacer varios alimentos y para experimentos químicos.
Lectura relacionada: Definición y Ejemplos de Quimioluminiscencia
Definición y Ejemplos de Quimioluminiscencia
Cómo Obtener Soda Cáustica o Lejía
Es mucho más difícil conseguir lejía de lo que solía ser en el pasado. La principal fuente de soda cáustica era la lejía Red Devil, pero ese producto ya no está en el mercado. ¿Por qué es difícil conseguir lejía? La razón es porque se puede usar para controlar el pH durante la producción de metanfetamina. Todavía hay algunas formas de obtener el químico. Asegúrese de que el producto sea 100% hidróxido de sodio, lejía o soda cáustica. Esto es especialmente importante si está elaborando alimentos, ya que un producto impuro puede contener contaminantes peligrosos. Las fuentes de lejía incluyen:
- Limpiador de desagües (revise la etiqueta), por ejemplo, Limpiador de desagües Roebic Crystal, que se vende en Lowes
- Hidróxido de sodio en una tienda de suministros químicos en línea
- Tienda de jabones
- Tienda de fabricación de velas
- Tienda de suministros de biodiesel
Ten en cuenta que, al comprar sosa cáustica o lejía, es posible que debas firmar una declaración de que no la estás usando para actividades ilegales. O bien, es posible que no necesite firmar nada, ya que una tarjeta de crédito proporciona prácticamente todos los detalles necesarios para encontrarlo si las autoridades piensan que es un narcotraficante en ascenso.
Lectura relacionada: Ejemplos de Propiedades Químicas
Ejemplos de Propiedades Químicas
Consejos Útiles
- Dado que es relativamente difícil conseguir este químico, es posible que deba comprarlo a granel. Es posible que pueda encontrar a otras personas que necesiten el producto químico para ayudar a dividir el costo. No es un artículo caro, pero probablemente no necesites varias libras de él.
- Mantenga el recipiente sellado y alejado de la humedad. La sosa cáustica absorbe y reacciona con el agua.
- Mantenga la lejía lejos de los niños y las mascotas. Tocarlo o ingerirlo puede causar una quemadura química potencialmente grave.
- Use guantes o utensilios para manipular la soda cáustica.
- Realice reacciones que involucren este químico en una habitación bien ventilada o al aire libre. La reacción libera calor y humos nocivos.
Sustitutos de Sosa Cáustica o Lejía
Dependiendo del propósito, es posible que pueda sustituir una base fuerte químicamente similar, el hidróxido de potasio (KOH). Este es un químico que puedes hacer, si eres extremadamente dedicado, remojando cenizas de madera en agua. Para hacer esto, remoje una gran cantidad de cenizas en una pequeña cantidad de agua. Espere aproximadamente una semana para que el agua extraiga la lejía. Drene el líquido, que contiene hidróxido de potasio, fíltrelo y hiérvalo para concentrar el álcali. Tenga cuidado y use guantes al manipular el líquido. El proyecto solo debe realizarse al aire libre o en un espacio bien ventilado.
Lectura relacionada: ¿Cuáles Son las Burbujas en el Agua Hirviendo?
¿Cuáles Son las Burbujas en el Agua Hirviendo?
Referencias Adicionales
- Brodale, G. E. y W. F. Giauque (1962). "La curva de solubilidad del punto de congelación del hidróxido de sodio acuoso en la región cercana al eutéctico de monohidrato anhidro." Revista de Química Física, volumen 66, número 10, pp. 2051-2051. doi: 10.1021 / j100816a051
- Deming, Horace G. (1925). Química General: Un Estudio Elemental Que Enfatiza las Aplicaciones Industriales de los Principios Fundamentales (2ª ed.). Nueva York: John Wiley & Sons, Inc.
- Haynes, William M., ed. (2011). Manual de Química y Física del CRC (92a ed.). Prensa CRC. ISBN 1439855110.
- O'Brien, Thomas F.; Bommaraju, Tilak V. Hine, Fumio (2005). Manual de Tecnología Cloroalcalina, vol. 1. Berlín, Alemania: Springer. Capítulo 2: Historia de la industria Cloroalcalina, p. 34. ISBN 9780306486241.
- Pickering, Spencer Umfreville (1893—: "LXI. - Los hidratos de sodio, potasio e hidróxidos de litio." Revista de la Sociedad Química, Transacciones, vol. 63, pp. 890-909. doi: 10.1039 / CT8936300890