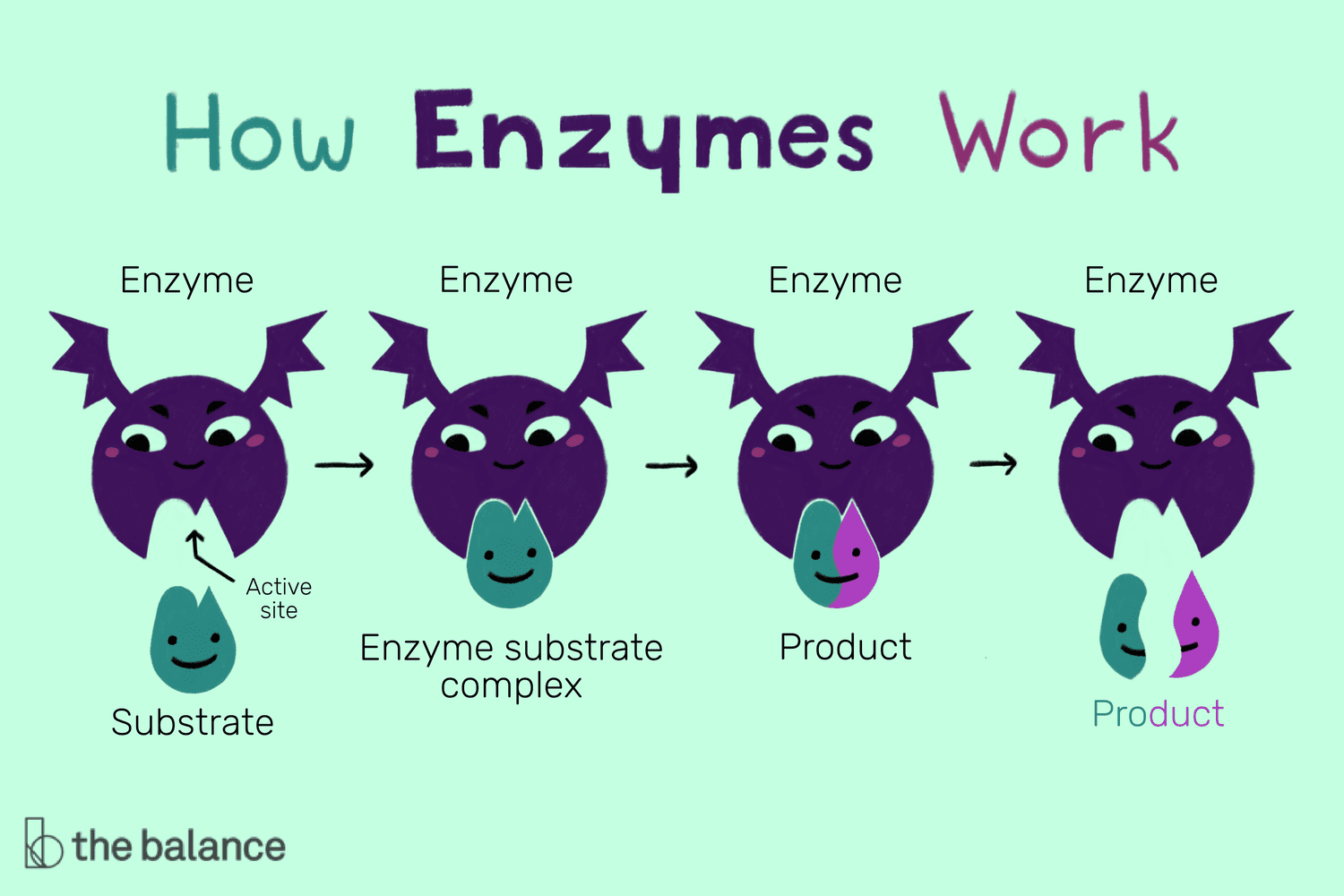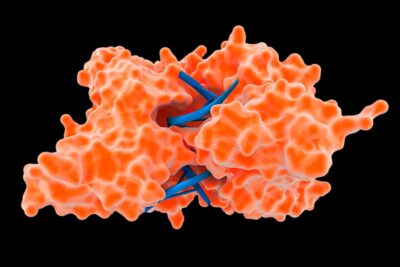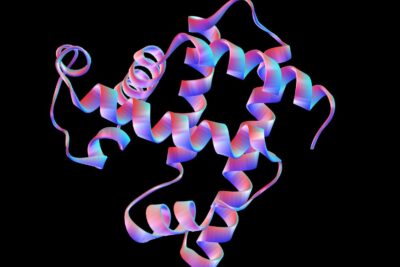
Una enzima es una proteína que facilita un proceso metabólico celular al disminuir los niveles de energía de activación (Ea) para catalizar las reacciones químicas entre biomoléculas. Algunas enzimas reducen la energía de activación a niveles tan bajos que en realidad revierten las reacciones celulares. Pero en todos los casos, las enzimas facilitan las reacciones sin alterarse, como la forma en que se quema el combustible cuando se usa.
Cómo Funcionan
Para que se produzcan reacciones químicas, las moléculas deben colisionar en las condiciones apropiadas que las enzimas pueden ayudar a crear. Por ejemplo, sin la presencia de una enzima apropiada, las moléculas de glucosa y las moléculas de fosfato en glucosa-6-fosfato permanecerán unidas. Pero cuando se introduce la enzima hidrolasa, las moléculas de glucosa y fosfato se separan.
Lectura relacionada: Cómo Medir el Volumen y la Densidad
Cómo Medir el Volumen y la Densidad
Composición
El peso molecular típico de una enzima (los pesos atómicos totales de los átomos de una molécula) varía de aproximadamente 10.000 a más de 1 millón. Un pequeño número de enzimas no son en realidad proteínas, sino que consisten en pequeñas moléculas de ARN catalítico. Otras enzimas son complejos multiproteínicos que comprenden múltiples subunidades proteicas individuales.
Si bien muchas enzimas catalizan reacciones por sí mismas, algunas requieren componentes no proteicos adicionales llamados "cofactores", que pueden ser iones inorgánicos como el Fe2+, Mg2+, Mn2+, o Zn2+, o pueden consistir en moléculas orgánicas o metaloorgánicas conocidas como "coenzimas"."
Lectura relacionada: El Órgano de Jacobson y el Sexto Sentido
El Órgano de Jacobson y el Sexto Sentido
Clasificación
La mayoría de las enzimas se clasifican en las siguientes tres categorías principales, según las reacciones que catalizan:
- Oxidorreductasas catalizan reacciones de oxidación en las que los electrones viajan de una molécula a otra. Un ejemplo: alcohol deshidrogenasa, que convierte alcoholes en aldehídos o cetonas. Esta enzima hace que el alcohol sea menos tóxico a medida que lo descompone, y también juega un papel clave en el proceso de fermentación.
- Transferasas catalizar el transporte de un grupo funcional de una molécula a otra. Los ejemplos primarios incluyen aminotransferasas, que catalizan la degradación de aminoácidos mediante la eliminación de grupos amino.
- Hidrolasa las enzimas catalizan la hidrólisis, en la que los enlaces sencillos se descomponen tras la exposición al agua. Por ejemplo, la glucosa-6-fosfatasa es una hidrolasa que elimina el grupo fosfato de la glucosa-6-fosfato, dejando glucosa y H3PO4 (ácido fosfórico).
Tres enzimas menos comunes son las siguientes:
Lectura relacionada: Ejemplos de Hipótesis Científicas
Ejemplos de Hipótesis Científicas- Liasas cataliza la descomposición de varios enlaces químicos por medios distintos a la hidrólisis y la oxidación, a menudo formando nuevos dobles enlaces o estructuras de anillo. La piruvato descarboxilasa es un ejemplo de una liasa que elimina el CO2 (dióxido de carbono) del piruvato.
- Isomerasas catalizan cambios estructurales en las moléculas, causando cambios en la forma. Un ejemplo: ribulosa fosfato epimerasa, que cataliza la interconversión de ribulosa-5-fosfato y xilulosa-5-fosfato.
- Ligasas catalizar la ligadura-la combinación de pares de sustratos. Por ejemplo, las hexoquinasas son una ligasa que cataliza la interconversión de glucosa y ATP con glucosa-6-fosfato y ADP.
Ejemplos en la Vida Cotidiana
Las enzimas afectan la vida cotidiana. Por ejemplo, las enzimas que se encuentran en los detergentes para ropa ayudan a degradar las proteínas que causan manchas, mientras que las lipasas ayudan a disolver las manchas de grasa. Las enzimas termotolerantes y criotolerantes funcionan a temperaturas extremas y, en consecuencia, son útiles para procesos industriales en los que se requieren altas temperaturas o para la biorremediación, que se producen en condiciones adversas, como las del Ártico.
En la industria alimentaria, las enzimas convierten el almidón en azúcar, con el fin de hacer edulcorantes de fuentes distintas de la caña de azúcar. En la industria de la confección, las enzimas reducen las impurezas en el algodón y reducen la necesidad de productos químicos potencialmente dañinos utilizados en el proceso de curtido del cuero.
Por último, la industria del plástico busca continuamente formas de utilizar enzimas para desarrollar productos biodegradables.