Un proceso químico reversible se considera en equilibrio cuando la velocidad de la reacción directa es igual a la velocidad de la reacción inversa. La relación de estas velocidades de reacción se denomina constante de equilibrio. Pon a prueba tus conocimientos sobre las constantes de equilibrio y su uso con esta prueba de práctica de constantes de equilibrio de diez preguntas.
Las respuestas aparecen al final de la prueba.
Pregunta 1
Una constante de equilibrio con un valor K & gt; 1 significa:
a. hay más reactivos que productos en equilibrio
b. hay más productos que reactivos en equilibrio
c. hay la misma cantidad de productos y reactivos en equilibrio
d. la reacción no está en equilibrio
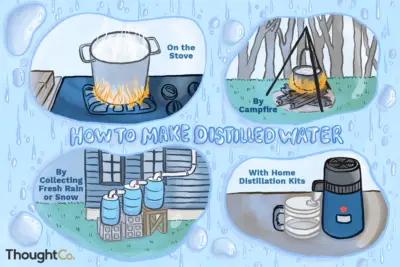
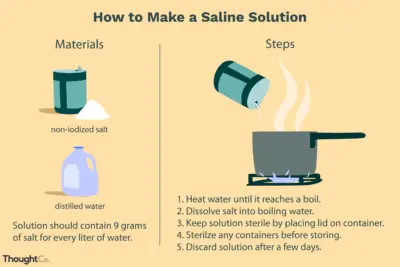
 Cómo La Liofilización Preserva El Material Biológico
Cómo La Liofilización Preserva El Material Biológico
Pregunta 2
Se vierten cantidades iguales de reactivos en un recipiente adecuado. Dado un tiempo suficiente, los reactivos pueden convertirse casi por completo en productos si:
a. K es menor que 1
b. K es mayor que 1
c. K es igual a 1
d. K es igual a 0
Lectura relacionada:
 Cómo Escribir un Informe de Proyecto de Feria de Ciencias
Cómo Escribir un Informe de Proyecto de Feria de CienciasPregunta 3
La constante de equilibrio para la reacción
H2 (g) + I2 (g) HI 2 HOLA (g)
sería:
a. K = [HI]2/[H2][I2]b. K = [H2][I2]/[HI]2
c. K = 2[HI]/[H2][I2]d. K = [H2][I2]/2[HI]
Pregunta 4
La constante de equilibrio para la reacción
2 ENTONCES2 (g) + O2 (g) SO 2 TAN3 g)
sería:
a. K = 2[SO3]/2[SO2][O2]b. K = 2[SO2][O2]/[SO3]c. K = [SO3]2/[SO2]2[O2]d. K = [SO2]2[O2]/[SO3]2
 Fosforilación y Cómo Funciona
Fosforilación y Cómo Funciona
Pregunta 5
La constante de equilibrio para la reacción
Ca (HCO3)2 (s) Ca CaO (s) + 2 CO2 (g) + H2O (g)
sería:
a. K = [CaO][CO2]2[H2O]/[Ca(HCO3)2]b. K = [Ca(HCO3)2]/[CaO][CO2]2[H2O]c. K = [CO2]2
d. K = [CO2]2[H2O]
Pregunta 6
La constante de equilibrio para la reacción
SnO2 (s) + 2 H2 g) S Sn (s) + 2 H2O (g)
sería:
a. K = [H2O]2/[H2]2
b. K = [Sn][H2O]2/[SnO][H2]2
c. K = [SnO][H2]2/[Sn][H2O]2
d. K = [H2]2/[H2O]2
Pregunta 7
Para la reacción
H2 (g) + Br2 (g ) HB 2 HBr (g),
K = 4,0 x 10-2. Para la reacción
2 HBr (g) H H2 (g) + Br2 g)
K =:
a. 4,0 x 10-2
b. 5
c. 25
d. 2,0 x 10-1
Pregunta 8
A una cierta temperatura, K = 1 para la reacción
2 HCl (g) → H2 (g) + Cl2 g)
En equilibrio, puedes estar seguro de que:
a. [H2] = [Cl2]b. [HCl] = 2[H2]c. [HCl] = [H2] = [Cl2] = 1
d. [H2][Cl2]/[HCl]2 = 1
Pregunta 9
Para la reacción: A + B C C + D
se mezclan juntos 6,0 moles de A y 5,0 moles de B en un recipiente adecuado. Cuando se alcanza el equilibrio, se producen 4,0 moles de C.
La constante de equilibrio para esta reacción es:
a. K = 1/8
b. K = 8
c. K = 30/16
d. K = 16/30
Pregunta 10
El proceso Haber es un método para producir amoníaco a partir de gases de hidrógeno y nitrógeno. La reacción es
N2 (g) + 3 H2 g) 2 NH3 g)
Si se añade gas hidrógeno después de que la reacción haya alcanzado el equilibrio, la reacción:
a. desplácese hacia la derecha para producir más producto
b. desplazarse hacia la izquierda para producir más reactivos
c. Detente. Todo el gas nitrógeno ya se ha agotado.
d. Necesita más información.
Respuestas
1. b. hay más productos que reactivos en equilibrio
2. b. K es mayor que 1
3. a. K = [HI]2/[H2][I2]4. c. K = [SO3]2/[SO2]2[O2]5. d. K = [CO2]2[H2O]6. a. K = [H2O]2/[H2]2
7. c. 25
8. d. [H2][Cl2]/[HCl]2 = 1
9. b. K = 8
10. a. desplácese hacia la derecha para producir más producto