Exploramos una lista de 10 bases comunes con estructuras químicas, fórmulas químicas y nombres alternativos.
Es vital entender que términos como fuerte y débil hacen referencia a la capacidad de disociación de la base en agua en iones componentes. Las bases fuertes se disociarán completamente, mientras que las bases débiles solo lo harán parcialmente.
Además, las bases de Lewis son aquellas capaces de donar un par de electrones a un ácido de Lewis. Estos 10 ejemplos de bases ilustran la variedad y la importancia de estas sustancias en diferentes campos de la química y la industria.
Acetona
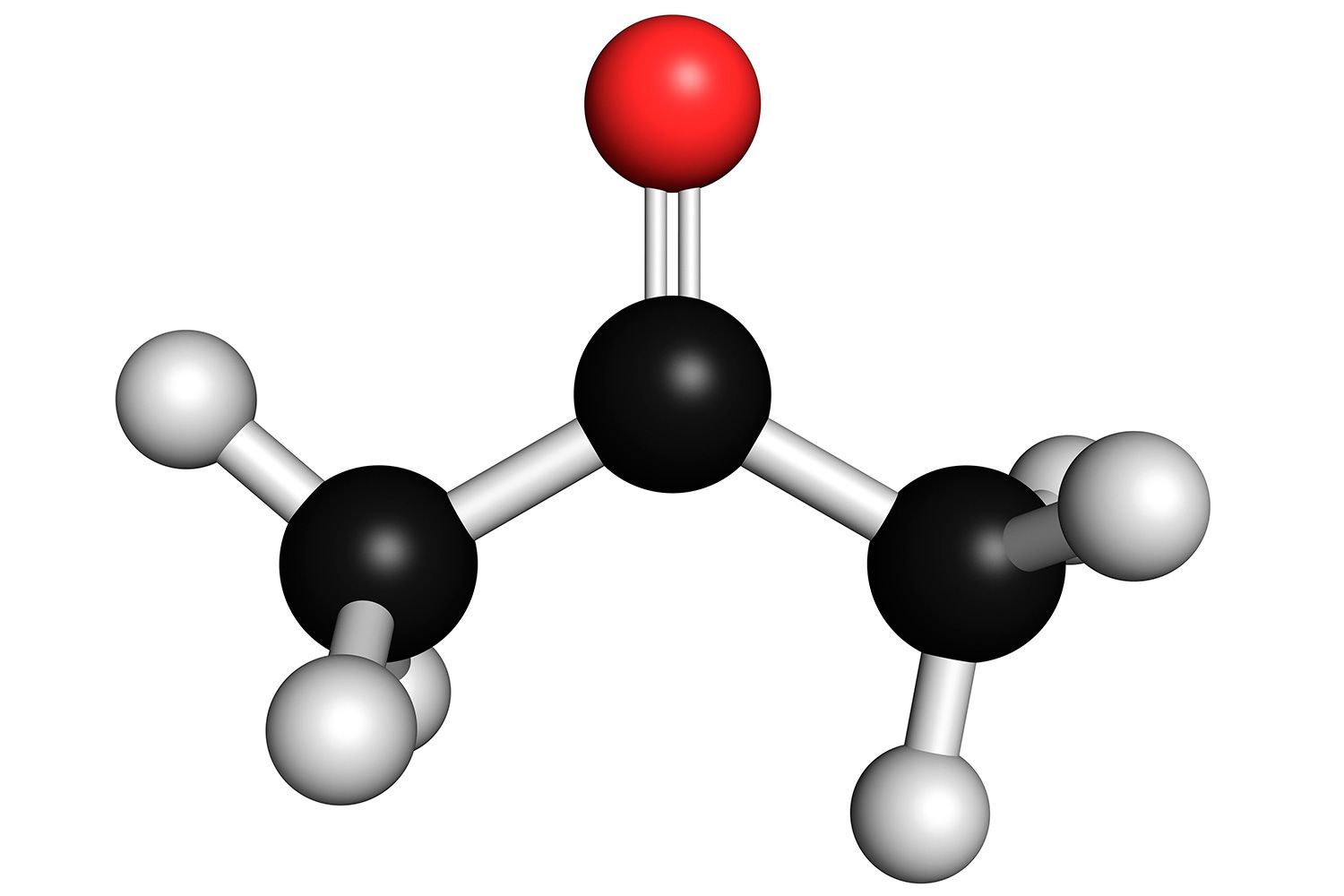
Esta es la estructura química de la acetona.
MOLEKUUL / Getty Images
Acetona: C3H6O
La acetona es una base de Lewis débil. También se conoce como dimetilcetona, azetón, β-cetopropano y propan-2-one. Es la molécula de cetona más simple. La acetona es un líquido volátil, inflamable e incoloro. Como muchas bases, tiene un olor reconocible.
 Hechos del Hidrógeno-H o Número atómico 1
Hechos del Hidrógeno-H o Número atómico 1
Amoníaco
Este es el modelo de bola y palo de la molécula de amoníaco.
Dorling Kindersley / Getty Images
Amoníaco: NH3
El amoníaco es una base de Lewis débil. Es un líquido o gas incoloro con un olor distintivo, utilizado en numerosos productos de limpieza y como refrigerante. Su importancia es tal que es considerado uno de los 10 ejemplos de mezclas homogéneas más significativos en la industria química.
Lectura relacionada:
 Diferencia Entre Radio Atómico y Radio Iónico
Diferencia Entre Radio Atómico y Radio IónicoHidróxido de Calcio
Esta es la estructura química del hidróxido de calcio.
Todd Helmenstine
Hidróxido de calcio: Ca(OH)2
El hidróxido de calcio es una base fuerte, conocida por su uso en la construcción y agricultura. Se disocia completamente en soluciones diluidas y tiene diversos nombres como hidrato de calcio y cal hidratada. Es bien conocido por su papel en la elaboración de mezclas homogéneas como la lechada de cal.
Hidróxido de Litio
Esta es la estructura química del hidróxido de litio.
Todd Helmenstine
Hidróxido de litio: LiOH
El hidróxido de litio es una base fuerte, aunque es la más débil entre los hidróxidos de metales alcalinos. Se utiliza principalmente en la síntesis de grasas lubricantes y en la purificación del aire en submarinos y naves espaciales. Este compuesto ilustra la diversidad funcional de nuestras 10 bases seleccionadas.
 Definición de Núcleo en Química
Definición de Núcleo en Química
Metilamina
Esta es la estructura química de la metilamina.
Ben Mills / PD
Metilamina: CH5N
La metilamina es una base de Lewis débil, encontrada frecuentemente como un gas incoloro y es la amina primaria más simple. Se utiliza en la producción de pesticidas, solventes y otros productos químicos. Su presencia en soluciones comunes manifiesta su lugar entre los 10 ejemplos de mezclas homogéneas en la industria.
Hidróxido de Potasio
Esta es la estructura química del hidróxido de potasio.
Todd Helmenstine
Hidróxido de potasio: KOH
El hidróxido de potasio es una base fuerte y una de las más comunes. Conocido también como potasa cáustica, se usa en una amplia gama de procesos, desde la fabricación de jabón hasta como limpiador de desagües. Su capacidad para formar soluciones alcalinas estables lo convierte en un componente esencial en la formulación de 10 ejemplos de bases para aplicaciones industriales.
Piridina
Esta es la estructura química de la piridina.
Todd Helmenstine
Piridina: C5H5N
La piridina es una base de Lewis débil, conocida por su olor a pescado que es desagradable para muchos. Es un líquido incoloro altamente inflamable y se utiliza como precursor en la síntesis de muchos productos farmacéuticos y agroquímicos. En el laboratorio, se emplea como solvente y reactivo, destacando su utilidad en este compendio de 10 bases.
Hidróxido de Rubidio
Esta es la estructura química del hidróxido de rubidio.
Todd Helmenstine
Hidróxido de rubidio: RbOH
El hidróxido de rubidio es una base fuerte que se prepara en el laboratorio. Es una sustancia altamente corrosiva y requiere el uso de equipo protector al manejarla. El hidróxido de rubidio es un ejemplo menos común, pero aun así, merece un lugar en nuestra lista de 10 ejemplos de bases por su utilidad en la investigación química.
Hidróxido de Sodio
Esta es la estructura química del hidróxido de sodio.
Todd Helmenstine
Hidróxido de sodio: NaOH
El hidróxido de sodio es una base fuerte, también conocida como lejía o soda cáustica. Es un sólido blanco extremadamente cáustico que se utiliza en una variedad de procesos, incluyendo la fabricación de jabón y como limpiador de desagües. Este compuesto es un claro representante de los 10 ejemplos de mezclas homogéneas al disolverse en agua, formando una solución uniforme.