Una reacción química es un proceso generalmente caracterizado por un cambio químico en el que los materiales de partida (reactivos) son diferentes de los productos. Las reacciones químicas tienden a involucrar el movimiento de electrones, lo que lleva a la formación y ruptura de enlaces químicos. Existen varios tipos diferentes de reacciones químicas y más de una forma de clasificarlas. A continuación, exploraremos algunos de los principales tipos de reacciones químicas ejemplos que nos ayudarán a comprender mejor esta fascinante área de la química.
Reacción de Oxidación-Reducción o Redox
En una reacción redox, se cambian los números de oxidación de los átomos. Las reacciones Redox pueden implicar la transferencia de electrones entre especies químicas. Uno de los 3 ejemplos de reacciones químicas de tipo redox es la que ocurre cuando I2 se reduce a I- y S2O32- (anión tiosulfato) se oxida a S4O62-:
2 S2O32−(aq) + I2(aq) → S4O62−(aq) + 2 I−(aq)
 Elementos en el Cuerpo Humano y Lo que Hacen
Elementos en el Cuerpo Humano y Lo que Hacen
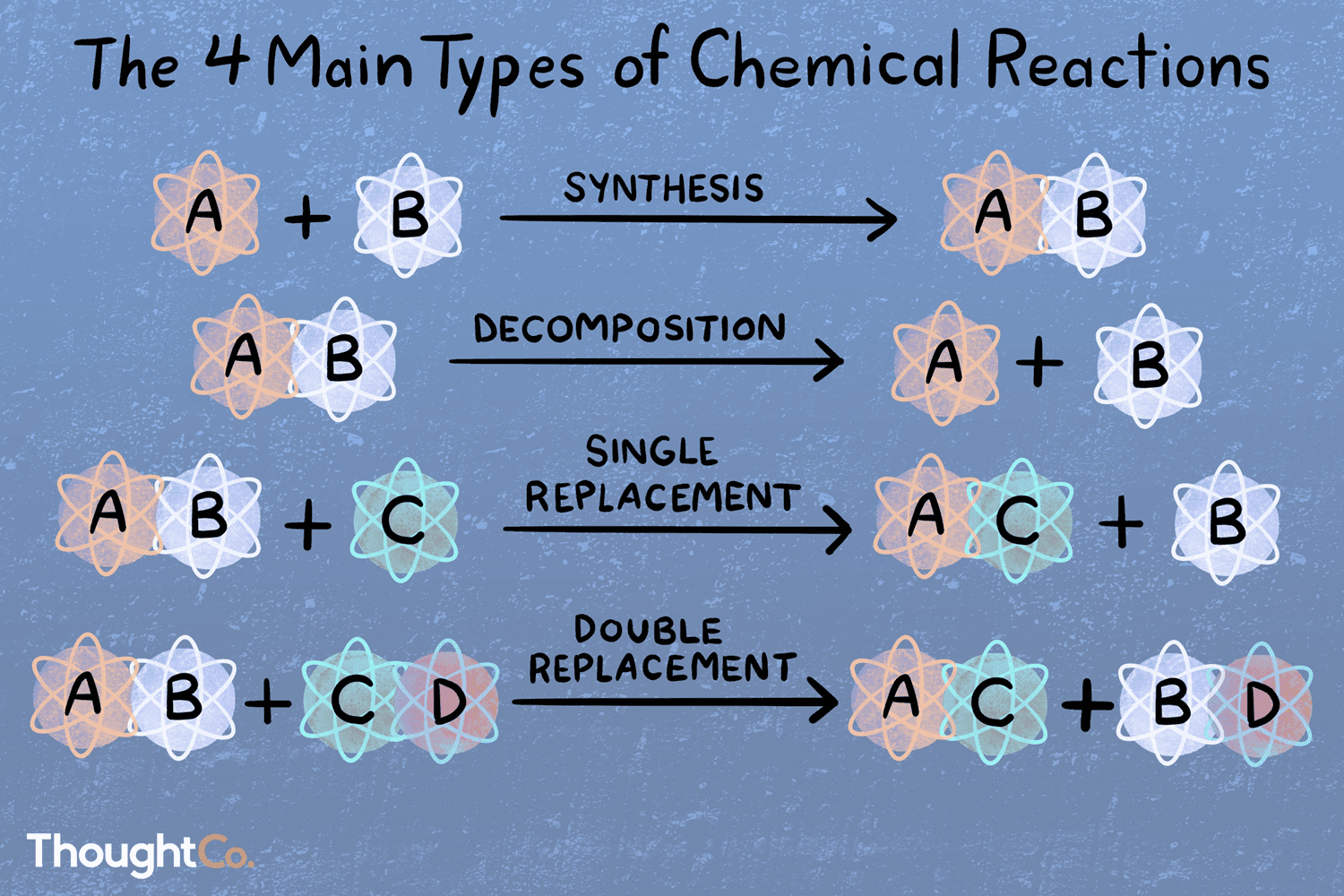
En una reacción de síntesis, dos o más especies químicas se combinan para formar un producto más complejo. A + B → AB. La combinación de hierro y azufre para formar sulfuro de hierro (II) es un ejemplo de una reacción de síntesis y uno de los 5 ejemplos de reacciones químicas comúnmente estudiados en química:
8 Fe + S8 → 8 FeS
Lectura relacionada:
 Composición Química de la Sal de Mesa
Composición Química de la Sal de MesaReacción de Análisis o Descomposición Química
En una reacción de descomposición, un compuesto se descompone en especies químicas más pequeñas. AB → A + B. La electrólisis del agua en oxígeno e hidrógeno gaseoso es un ejemplo de reacción de descomposición y forma parte de los 10 ejemplos de reacciones químicas que se pueden observar tanto en laboratorios como en aplicaciones industriales:
2 H2O → 2 H2 + O2
Reacción de Desplazamiento Único o Sustitución
Una reacción de sustitución o de desplazamiento único se caracteriza por que un elemento es desplazado de un compuesto por otro elemento. A + BC → AC + B. Un ejemplo de una reacción de sustitución ocurre cuando el zinc se combina con ácido clorhídrico. El zinc reemplaza al hidrógeno, y este proceso es parte de los 10 ejemplos de reacciones químicas que se enseñan comúnmente en la educación química:
Zn + 2 HCl → ZnCl2 + H2
 10 Tipos Comunes de Corrosión
10 Tipos Comunes de Corrosión
Metátesis o Reacción de Doble Desplazamiento
En una reacción de doble desplazamiento o metátesis, dos compuestos intercambian enlaces o iones para formar compuestos diferentes. AB + CD → AD + CB. Un ejemplo de una reacción de doble desplazamiento se produce entre el cloruro de sodio y el nitrato de plata para formar nitrato de sodio y cloruro de plata. Este es otro de los 5 ejemplos de reacciones químicas que demuestran la diversidad de las transformaciones químicas:
NaCl (aq) + AgNO3(aq) → NaNO3(aq) + AgCl(s)
Reacción Ácido-Base
Una reacción ácido-base es un tipo de reacción de doble desplazamiento que ocurre entre un ácido y una base. La H+ el ion en el ácido reacciona con el OH- ion en la base para formar agua y una sal iónica: HA + BOH → H2O + BA. La reacción entre el ácido bromhídrico (HBr) y el hidróxido de sodio es un ejemplo de una reacción ácido-base y se incluye en la lista de 3 ejemplos de reacciones químicas esenciales en el estudio de la química:
HBr + NaOH → NaBr + H2O
Una reacción de combustión es un tipo de reacción redox en la que un material combustible se combina con un oxidante para formar productos oxidados y generar calor (reacción exotérmica). Normalmente, en una reacción de combustión, el oxígeno se combina con otro compuesto para formar dióxido de carbono y agua. Un ejemplo de reacción de combustión y uno de los 10 ejemplos de reacciones químicas más espectaculares es la combustión de naftaleno:
C10H8 + 12 O2 → 10 CO2 + 4 H2O
Isomerización
En una reacción de isomerización, la disposición estructural de un compuesto cambia, pero su composición atómica neta sigue siendo la misma. La isomerización del butano en isobutano es un ejemplo de reacción de isomerización, y se cuenta entre los 5 ejemplos de reacciones químicas que muestran cómo pueden variar las estructuras de los compuestos sin cambiar su fórmula molecular.
Reacción de Hidrólisis
Una reacción de hidrólisis implica agua. La forma general para una reacción de hidrólisis es: X-(aq) + H2O (l ) → HX (aq) + OH-(aq). Un ejemplo de reacción de hidrólisis es la conversión de ésteres en alcoholes y ácidos, un proceso vital que se incluye en la lista de 10 ejemplos de reacciones químicas que son fundamentales en bioquímica y síntesis orgánica.
Los Principales Tipos De Reacción
¡Hay cientos o incluso miles de tipos de reacciones químicas! Si se le pide que nombre los principales tipos de reacciones químicas, aquí tiene una clasificación. Los cuatro tipos principales de reacciones son combinación directa, reacción de análisis, desplazamiento único y doble desplazamiento. Si se pregunta por los cinco tipos principales de reacciones, son estos cuatro y luego ácido-base o redox (dependiendo de a quién le pregunte). Tenga en cuenta que una reacción química específica puede pertenecer a más de una categoría. Además, como parte de nuestro enfoque educativo, presentamos 10 ejemplos de reacciones químicas que ilustran la diversidad y la complejidad de estas transformaciones en la química.